Инженерный тур. 1 этап
- Условие
Какое из приведенных веществ не является природным полимером?
- ДНК.
- Хитин.
- Органическое стекло.
- Крахмал.
Решение- ДНК — природный полимер, состоящий из нуклеотидов в качестве мономеров.
- Хитин — полисахарид, длинноцепочечный полимер N-ацетилглюкозамина, амидного производного глюкозы.
- Органическое стекло — тривиальное название вещества, получаемого из полиметилметакрилата.
- Крахмал — смесь полисахаридов амилозы и амилопектина, мономером которых является альфа-глюкоза.
ОтветC.
- Условие
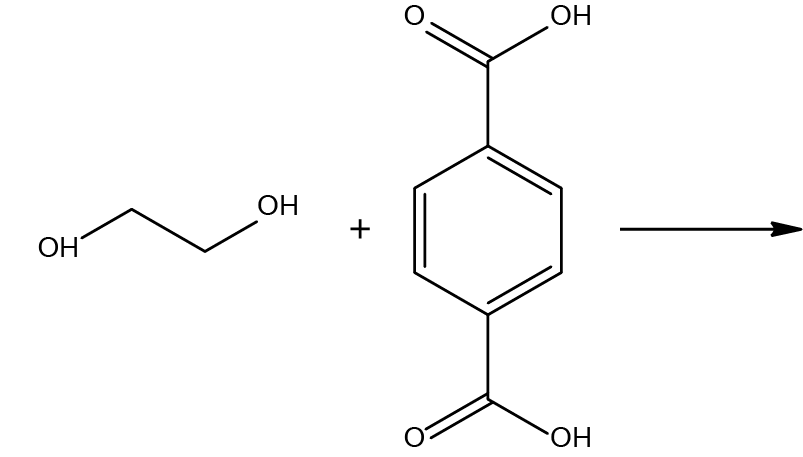
Какой из приведенных полимеров образуется в данной реакции?
Рис. 1.1.- Полистирол.
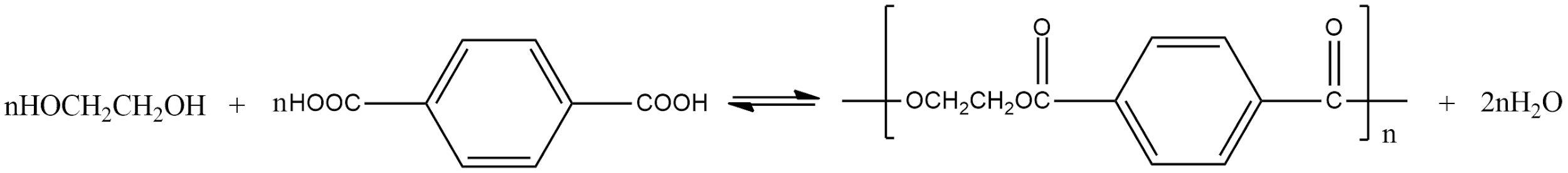
- Полиэтилентерефталат.
- Фенолформальдегидная смола.
- Капрон.
РешениеПродуктом реакции поликонденсации этиленгликоля и терефталиевой кислоты является полиэтилентерефталат.
ОтветB.
- Условие
Какое из приведенных веществ является мономером натурального каучука?
- Этилен.
- Пропилен.
- Бутадиен.
- Изопрен.
РешениеНатуральный каучук — природный полимер, получаемый полимеризацией изопрена, который содержится в млечном соке некоторых тропических растений.
ОтветD.
- Условие
Выберите неверное утверждение о стадиях полимеризации.
- Инициирование — зарождение активных центров полимеризации.
- Рост цепи — процесс последовательного присоединения молекул мономеров к центрам.
- Разветвление цепи — образование нескольких активных центров из одного.
- Обрыв цепи — переход активного центра на другую молекулу.
РешениеОбрывом цепи называют стадию гибели активных центров, а переходом активного центра на другую молекулу является стадия передачи цепи.
ОтветD.
Промышленный синтез полиамидов играет очень важную роль в современном производстве и улучшении качества жизни, обеспечивая высокопрочные и надежные материалы для различных нужд. Так, например, полиамиды широко применяются в строительстве, медицине и в электронике.
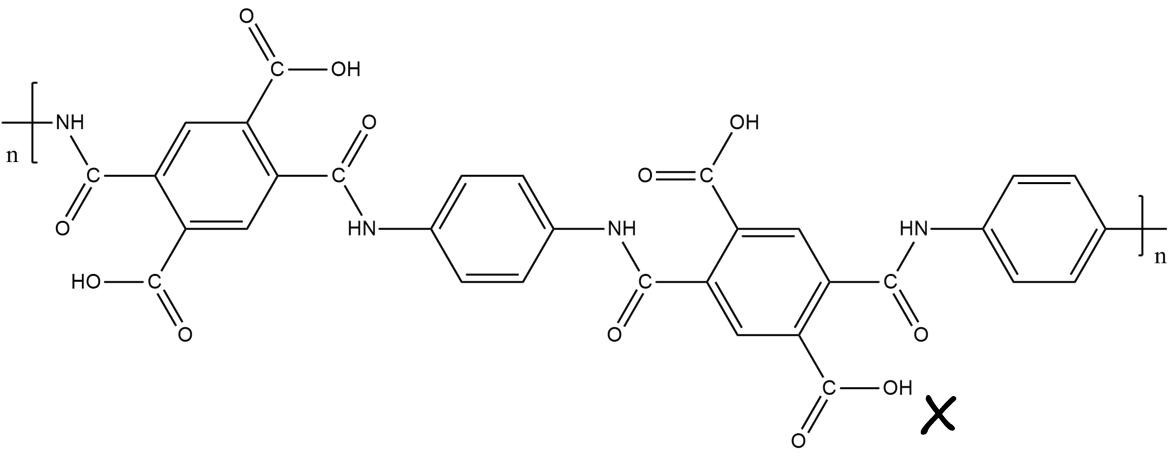
Рассмотрите схему синтеза полиамида X (рис. 1.2), который отличается хорошей термостойкостью: температура его размягчения выше 800 °C.
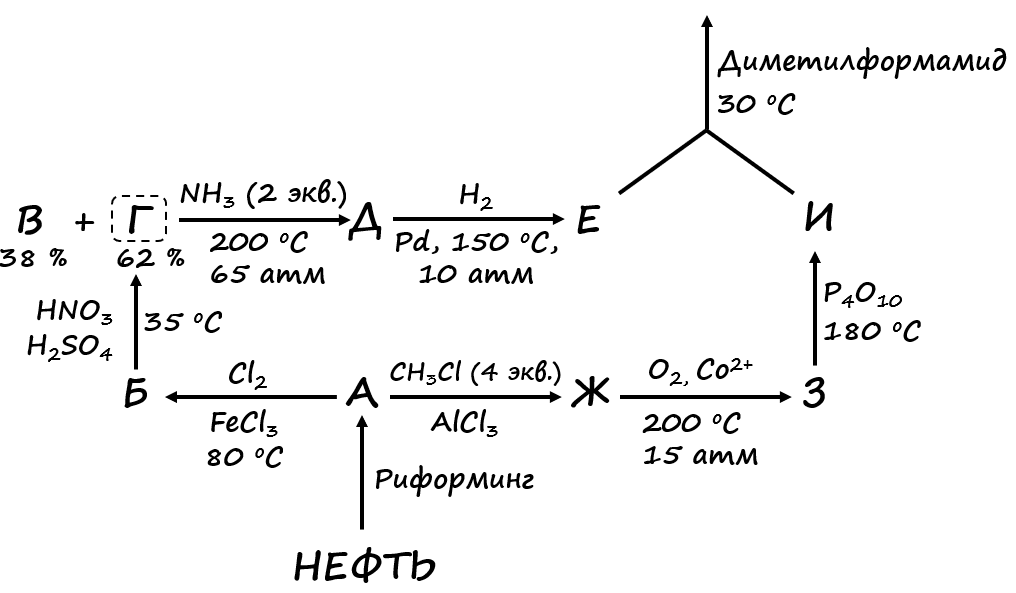
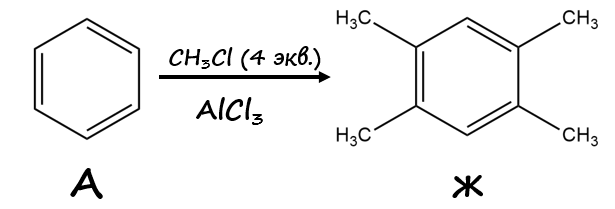
Вещество A (рис. 1.3), выделяемое из нефти риформингом, относится к ряду ароматических веществ, а его верная структура впервые была предложена в 1865 году немецким химиком Фридрихом Кекуле. Содержание углерода по массе в соединении A составляет 92,31%.
Спектр ЯМР 1H высокосимметричного вещества Ж, получаемого из A алкилированием по Фриделю – Крафтсу, показал, что соединение содержит два типа атомов водорода в соотношении \(6 : 1\). Вещества В и Г — изомеры, образующиеся после нитрования Б. На схеме (рис. 1.3) указаны их массовые доли в изомерной cмеси. В цепочке превращений участвует именно вещество Г, из которого получают Д, содержащее 52,17% углерода по массе. Расшифруйте структуры веществ A – И.
Ароматическое вещество A, верная структура которого была предложена Кекуле в 1865 году — бензол, рис. 1.4.
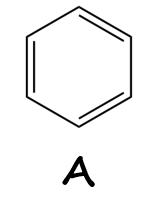
Это подтверждается и массовым содержанием углерода в \(\ce{C6H6}\): \[\omega(C)= \frac{12 \cdot 6}{12 \cdot 6+6}=0{,}9231.\]
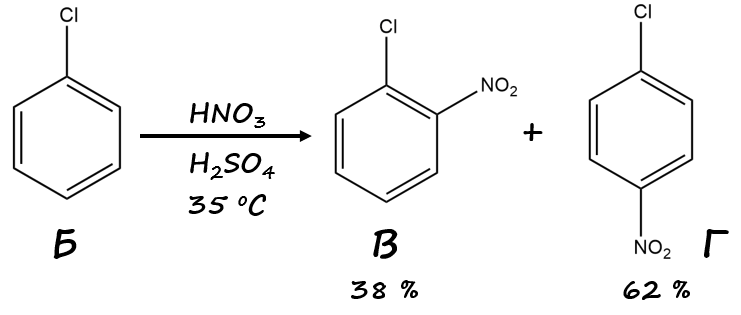
Хлорирование бензола с использованием хлорида железа (III) (как катализатора хлорирования по Фриделю – Крафтсу) приводит к веществу Б — хлорбензолу (рис. 1.5),
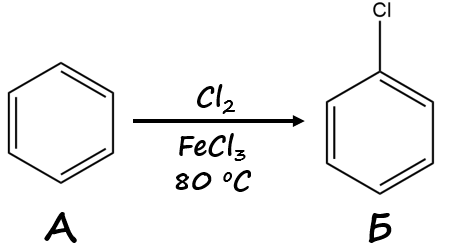
который затем нитруется до изомеров — 2-нитрохлорбензола и 4-нитрохлорбензола (рис. 1.6),
причем, именно 4-нитрохлорбензол — это вещество Г как более выгодный пара-изомер. 4-нитрохлорбензол аммонируется под высокой температурой и давлением, образуя амин (рис. 1.7).
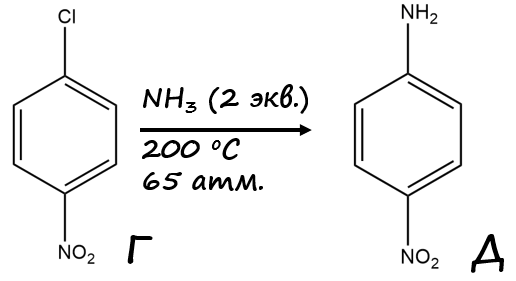
Образование амина подтверждается содержанием углерода в нем: \[\omega(C)= \frac{12 \cdot 6}{12 \cdot 6+14 \cdot 2+16 \cdot 2+6 }=0{,}5217.\]
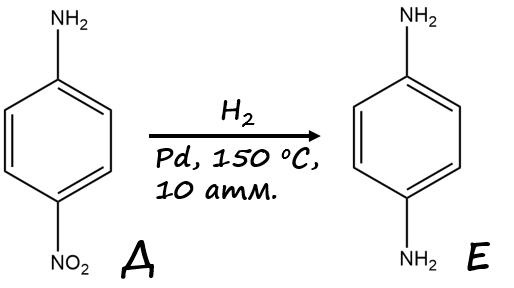
Вывод о структуре вещества Д можно сделать и по приведенной структуре полимера X. Получившееся вещество Д гидрируется на палладиевом катализаторе, в результате чего образуется п-фенилдиамин — вещество Е, рис. 1.8.
Далее расшифруем структуру соединения Ж. Оно получается в результате алкилирования бензола по Фриделю – Крафтсу, причем, стоит обязательно обратить внимание на то, что на схеме бензол и хлорметил вступают во взаимодействие в соотношении \(1 : 4\). Данные спектра ЯМР 1H говорят о том, что в структуре Ж содержатся два типа атомов водорода в соотношении \(6 : 1\). Учитывая высокую симметричность соединения, нетрудно догадаться о том, что это 1,2,4,5-тетраметилбензол (рис. 1.9),
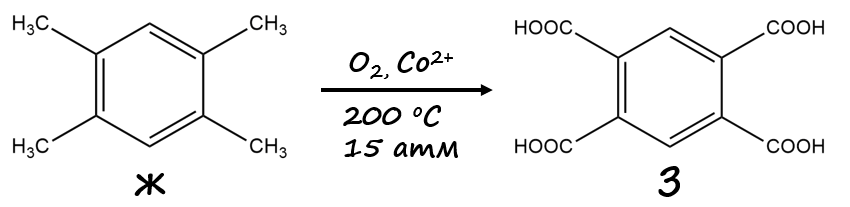
который окисляется кислородом до четырхосновной кислоты (рис. 1.10),
которая затем под действием оксида фосфора (V) теряет воду и переходит в свой ангидрид И (рис. 1.11),
который затем полимеризуется с полученным ранее п-фенилдиамином в диметилформамиде, образуя полиамид Х.
- Условие
Какой из перечисленных методов анализа является наиболее доступным?
- Масс-спектрометрия.
- Титриметрия.
- Рентгенография (рентгено-структурный анализ).
- ЯМР (ядерно-магнитный резонанс).
РешениеТитриметрия — это классический химический метод количественного анализа, основанный на измерении объема реактива, необходимого для завершения химической реакции с анализируемым веществом. Метод требует минимального оборудования (бюретки, мерные колбы и реагенты), что делает его значительно дешевле в сравнении с такими высокотехнологичными методами, как масс-спектрометрия, рентгенография или ЯМР, для реализации которых необходимо сложное дорогостоящее оборудование и значительные затраты на его обслуживание.
ОтветB.
- Условие
Какая мера может наилучшим образом помочь снизить ошибку при титровании?
- Максимально увеличить величину скачка и правильно выбрать индикатор.
- Использовать более концентрированные растворы для титрования.
- Использовать масс-спектрометр.
- Использовать при анализе вторичный стандарт.
Решение- Может значительно помочь в снижении ошибки, так как правильный выбор индикатора и увеличение величины скачка позволяют более точно определить момент окончания реакции. Индикатор должен давать четкий и видимый переход, его подбор крайне важен.
- Может, наоборот, увеличить ошибку. Более концентрированные растворы приводят к резкому протеканию реакции, что может затруднить точное определение конечной точки титрования. Кроме того, такие растворы менее стабильны.
- Масс-спектрометрия — это метод анализа, при помощи которого, измеряя отношение массы к заряду ионов анализируемого вещества, можно идентифицировать его качественный состав (вплоть до структуры молекулы). В теории можно попробовать этот метод, ориентируясь на концентрацию детектируемых ионизированных частиц, но это крайне дорогой, долгий и, самое главное, неточный процесс.
- Вторичный стандарт используется, когда первичный недоступен, он может внести дополнительные ошибки в количественное определение. Его использование нецелесообразно, если доступен первичный стандарт.
ОтветA.
- Условие
В условиях анализа жесткости воды титриметрическим методом чем является раствор комплексона-III?
- Индикатором.
- Титрируемым веществом.
- Титрантом.
- Аликвотой.
РешениеТитрант — это вещество, которое добавляют из бюретки в процессе титрования для определения концентрации анализируемого вещества. В анализе жесткости воды комплексон-III (ЭДТА) используется для комплексообразования с ионами кальция и магния, которые в основном задают жесткость воды. Поэтому он выполняет роль титранта.
ОтветС.
- Условие
Для стандартизации раствора гидроксида калия были взяты три навески дигидрата щавелевой кислоты массой \(0{,}300\), \(0{,}400\) и \(0{,}501\) г. В результате кислотно-основного титрования в присутствии фенолфталеина было израсходовано \(5{,}900\), \(8{,}100\), \(12{,}600\) мл раствора щелочи соответственно. Определите концентрацию раствора в молях на литр гидроксида калия, исходя из полученных данных. Промежуточные результаты и ответ округлите до третьей значащей цифры.
РешениеРеакция: \[\ce{H2C2O4} + 2\ce{KOH} \rightarrow \ce{K2C2O4} + 2\ce{H2O}.\]
Замечаем, что третье титрование сильно не сходится с первыми двумя. Значит, не учитываем его в дальнейших расчетах.
Сначала найдем количество вещества щавелевой кислоты в каждой из навесок: \[\frac{m(\ce{H2C2O4} \cdot 2\ce{H2O})}{M(\ce{H2C2O4} \cdot 2\ce{H2O})} = n(\ce{H2C2O4} \cdot 2\ce{H2O}).\]
Получаем 0,00238, 0,00317 моль соответственно.
С учетом того, что моли гидроксида калия в реакции нейтрализации находятся в соотношении \(2:1\) к молям кислоты, можем найти концентрацию раствора щелочи исходя из трех экспериментов: \[C(\ce{KOH}) = \frac{n(\ce{H2C2O4} \cdot 2\ce{H2O}) \cdot 2}{V(\ce{NaOH})}.\]
Получаем: 0,807 М, 0,783 М.
Среднее арифметическое: 0,795 М.
Ответ\(0{,}795 \pm 0{,}050\) М.
- Условие
В кулинарии в качестве разрыхлителя теста может использоваться смесь карбоната аммония и гидрокарбоната натрия. Чтобы понять, в каком соотношении находятся вещества в подобных разрыхлителях, был проведен титриметрический анализ. На титрование навески разрыхлителя массой 0,500 г, состоящей только из карбоната аммония и гидрокарбоната натрия, ушло 10 мл \(\ce{HCl}\) (C = 0,833 М). Определите массовые доли солей в смеси.
РешениеРеакции: \[(\ce{NH_4})_2\ce{CO_3} + 2\ce{HCl} \rightarrow 2\ce{NH_4}\ce{Cl} + \ce{H2O} + \ce{CO_2};\] \[\ce{NaHCO_3} + \ce{HCl} \rightarrow \ce{NaCl} + \ce{H2O} + \ce{CO_2}.\]
Составляем систему уравнений: \[\left\{ \begin{aligned} X + 2Y &= 0{,}833 \cdot 0{,}01, \\ 84X + 96Y &= 0{,}5, \end{aligned} \right.\] где \(X\) — количество моль гидрокарбоната натрия, \(Y\) — количество моль карбоната аммония.
Получаем: 0,234 г гидрокарбоната натрия и 0,266 г карбоната аммония.
Массовые доли: 46,8% и 53,2% соответственно.
Ответ\(46{,}8 \pm 0{,}5\)%, \(53{,}2 \pm 0{,}5\)%.
- Условие
Далеко не всегда представляется возможным выделить полимер из реакционной смеси и определить его массу или процент превращения.
В случае поликонденсации адипиновой кислоты с этиленгликолем в расплаве метод определения степени конверсии и схема реакции выглядят следующим образом, рис. 1.12.
Рис. 1.12.Первую пробу отбирают после образования гомогенного расплава. Для этого в смесь вводят стеклянный стержень, отбирают небольшую пробу и переносят в стакан для титрования. После добавления спирта и хлороформа полимер растворяют и проводят титрование в присутствии тимолфталеина спиртовым раствором гидроксида калия. По каплям добавлять щелочь продолжают до нейтральной реакции среды — о ней будет свидетельствовать появление синей окраски, не пропадающей в течение 20 с при интенсивном перемешивании. Далее пробу отбирают еще несколько раз каждые 10 мин (то есть вторая проба была отобрана через 10 мин после начала эксперимента и т. д.).
После записи результатов в таблицу можно определить кислотное число (КЧ) проб. За \(\text{КЧ}_0\) возьмем результат для первой пробы. Формула для расчета: \[\text{КЧ} = \frac{m_{\text{KOH}}}{m_{\text{образца}}},\] то есть количество миллиграммов KOH, необходимое для титрования 1 г реакционной смеси.
В результате серии экспериментов были получены следующие результаты:
- массы образцов: 6, 6,1, 6,2, 5,8 г.
- объемы KOH: 10,1, 3,3, 2, 1,3 мл.
Для нахождения степени конверсии \(q\) используйте формулу: \[q = \frac{\text{КЧ}_0 - \text{КЧ}}{\text{КЧ}_0} \cdot 100\%.\]
Учитывая, что концентрация KOH равна 0,01 моль/л, найдите степень полимеризации спустя 20 мин после начала эксперимента.
РешениеСпустя 20 мин отбирается третья проба, значит, сначала находим \(\text{КЧ}_0\): \[\text{КЧ}_0 = \frac{C_{\text{KOH}} \cdot V_{\text{KOH}} \cdot M_{\text{KOH}}}{m_{\text{образца}}} = \frac{0{,}01 \cdot 0{,}0101 \cdot 56}{6} \cdot 1000 = 0{,}943 \, \text{мг/г}.\]
Аналогично находим \(\text{КЧ}\) для третьей пробы: \[\text{КЧ} =\frac{C_{\text{KOH}} \cdot V_{\text{KOH}} \cdot M_{\text{KOH}}}{m_{\text{образца}}}= \frac{0{,}01 \cdot 0{,}002 \cdot 56}{6{,}2} \cdot 1000 = 0{,}181 \, \text{мг/г}.\]
Значит, степень конверсии \(q\) равна: \[q = \frac{0{,}943 - 0{,}181}{0{,}943} \cdot 100\% = 80{,}8\%.\]
Ответ\(80{,}8 \pm 0{,}5\)%.
- УсловиеВыберите верный вариант: электромагнитная волна с большей длиной волны обладает...
- большей энергией,
- меньшей энергией,
- большей частотой,
- меньшей скоростью.
ОтветB.
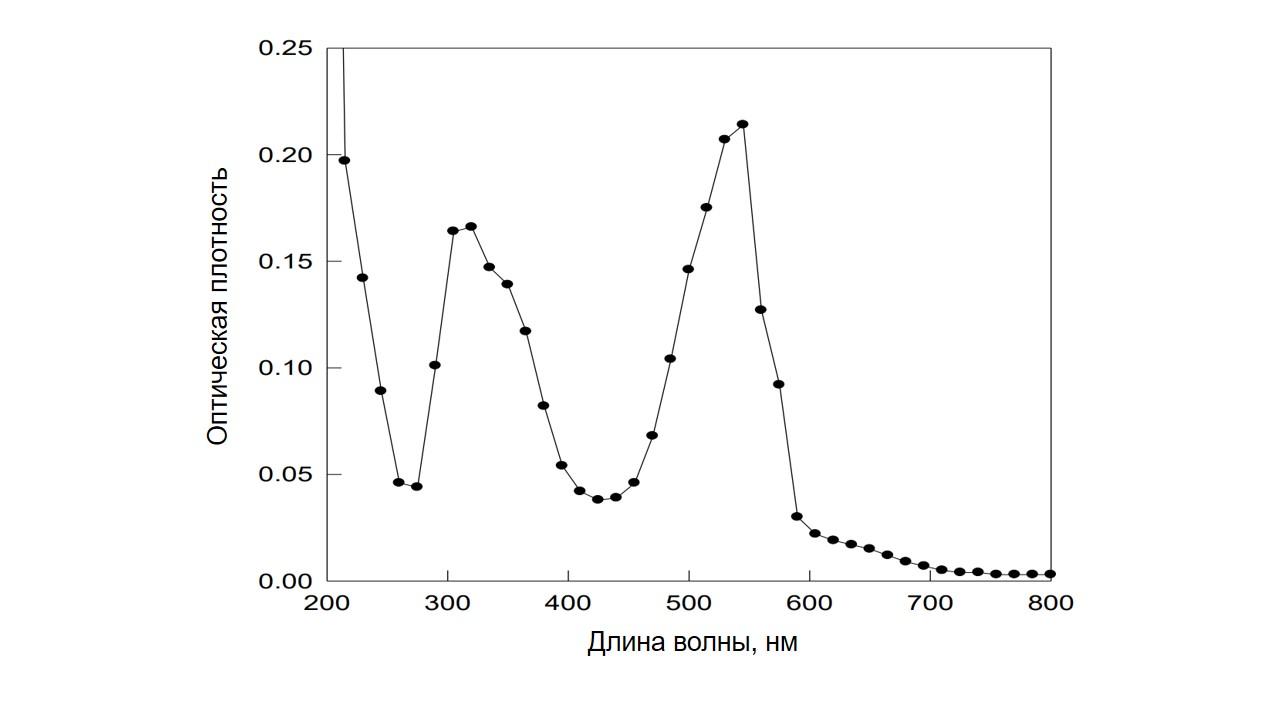
- УсловиеОптический спектр раствора какого вещества приведен на рис. 1.13?Рис. 1.13.
- Сульфат меди (II).
- Хлорид железа (III).
- Перманганат калия.
- Сульфат никеля (II).
ОтветC.
- УсловиеСпектрофотометрическое определение концентрации металла в руде является примером...
- неинструментального метода анализа,
- полуколичественного анализа,
- количественного анализа,
- качественного анализа.
ОтветC.
- УсловиеСанитарный контроль пищевого полистирола
Обычно свойства полимеров и исходных мономеров значительно отличаются: в то время как контакт с полимером не несет непосредственных последствий для здоровья человека, мономеры часто представляют собой токсичные вещества — поэтому очень важно контролировать их остаточное содержание в материалах.
Изделия из полистирола широко используются в самых различных областях: от теплоизоляционных плит и детских игрушек до одноразовых шприцев, катетеров и пищевой упаковки. Из разных марок полистирола производят стаканчики для йогуртов, одноразовые контейнеры и посуду, упаковку для яиц и подложки. Важно проверять допустимые условия использования, поскольку при действии высокой температуры (например, при контакте с горячим напитком или разогреве в микроволновой печи) может происходить частичная деполимеризация с выделением токсичного стирола.
 Рис. 1.14.
Рис. 1.14.Определение содержания остаточного стирола в полистироле можно проводить спектрофотометрическим методом, при этом измерение оптической плотности проводят не для водных растворов, а для экстрактов в гексане.
Образец полимера (полистирол суспензионный ПС-С) массой 35,200 г вымачивали в 200 мл дистиллированной воды на протяжении 10 сут. Далее к полученной воде пипеткой добавили 10,0 мл гексана и осторожно взбалтывали 6 мин для перехода стирола в гексан, выдержали раствор 30 мин. После разделения водной и органической фазы гексановый слой (раствор X) отобрали и измерили его оптическую плотность при длине волны 247 нм относительно чистого гексана.
Также приготовили серию стандартных растворов 1–5: для этого к образцам воды по 200 мл добавили известное количество чистого стирола и провели экстракцию 10,0 мл гексана аналогичным образом, их оптическую плотность измерили.
Используя данные таблицы 1, определите массовую долю в процентах остаточного стирола в образце полистирола с точностью до тысячных, учитывая, что вода и гексан стирола не содержали, органические примеси в экстракте из полимера не поглощают излучение при выбранной длине волны. Сравните результат с допустимым значением 0,05%.
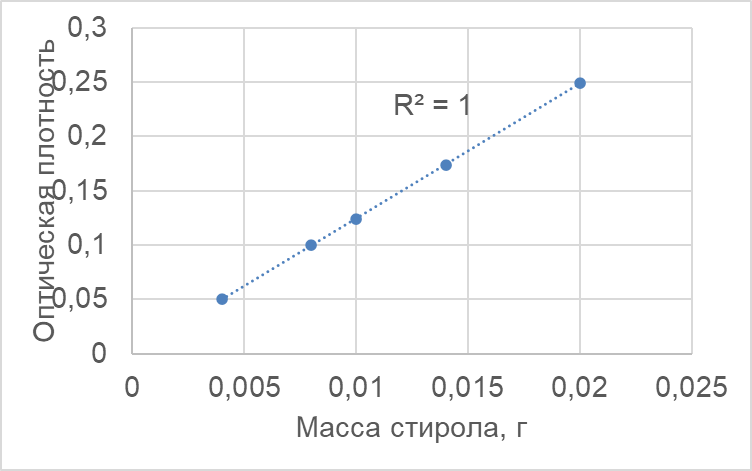
Раствор Масса добавленного стирола, мг Оптическая плотность 1 0,004 0,050 2 0,008 0,099 3 0,010 0,124 4 0,014 0,174 5 0,020 0,248 \(X\) 0,180 РешениеРис. 1.15.Зависимость оптической плотности экстракта связана с концентрацией вещества линейно по закону Бугера – Ламберта – Бера, а поскольку объемы растворов одинаковы, то это можно применить и к массе стирола: \[A=\varepsilon lc= \frac{\varepsilon l}{V} m=km,\] где \(k\) — некоторый коэффициент. Коэффициент \(k\) определим с помощью построения графика, рис. 1.15.
\(k = 12{,}43\) г\(^{-1}\), откуда масса стирола в экстракте \(X\) составляет: \[m=\frac{0{,}185}{12{,}43}=0{,}015~\text{г},\] то есть массовая доля стирола в полистироле составляет: \[\omega=\frac{0{,}015}{35{,}200}=0{,}042\%.\]
Ответ\(0{,}042\pm 0{,}001\).
- УсловиеЦифрами 1–4 обозначены инфракрасные спектры пропускания: по оси ординат приведены значения оптической плотности, по оси абсцисс — волновые числа в обратных сантиметрах (см\(^{-1}\)). Сопоставьте инфракрасные спектры и соответствующие им полимеры, используя представленные структурные формулы полимеров. В ответе укажите последовательность букв, отвечающую полимерам.
ИК-спектры:
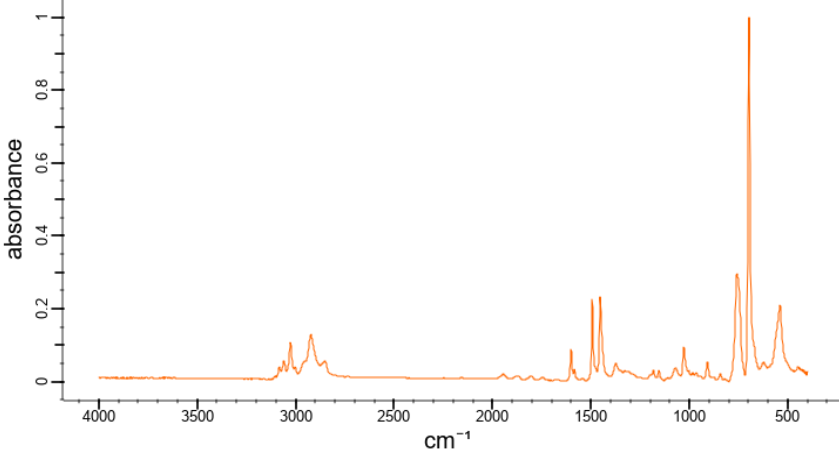
- Спектр 1
- Спектр 2
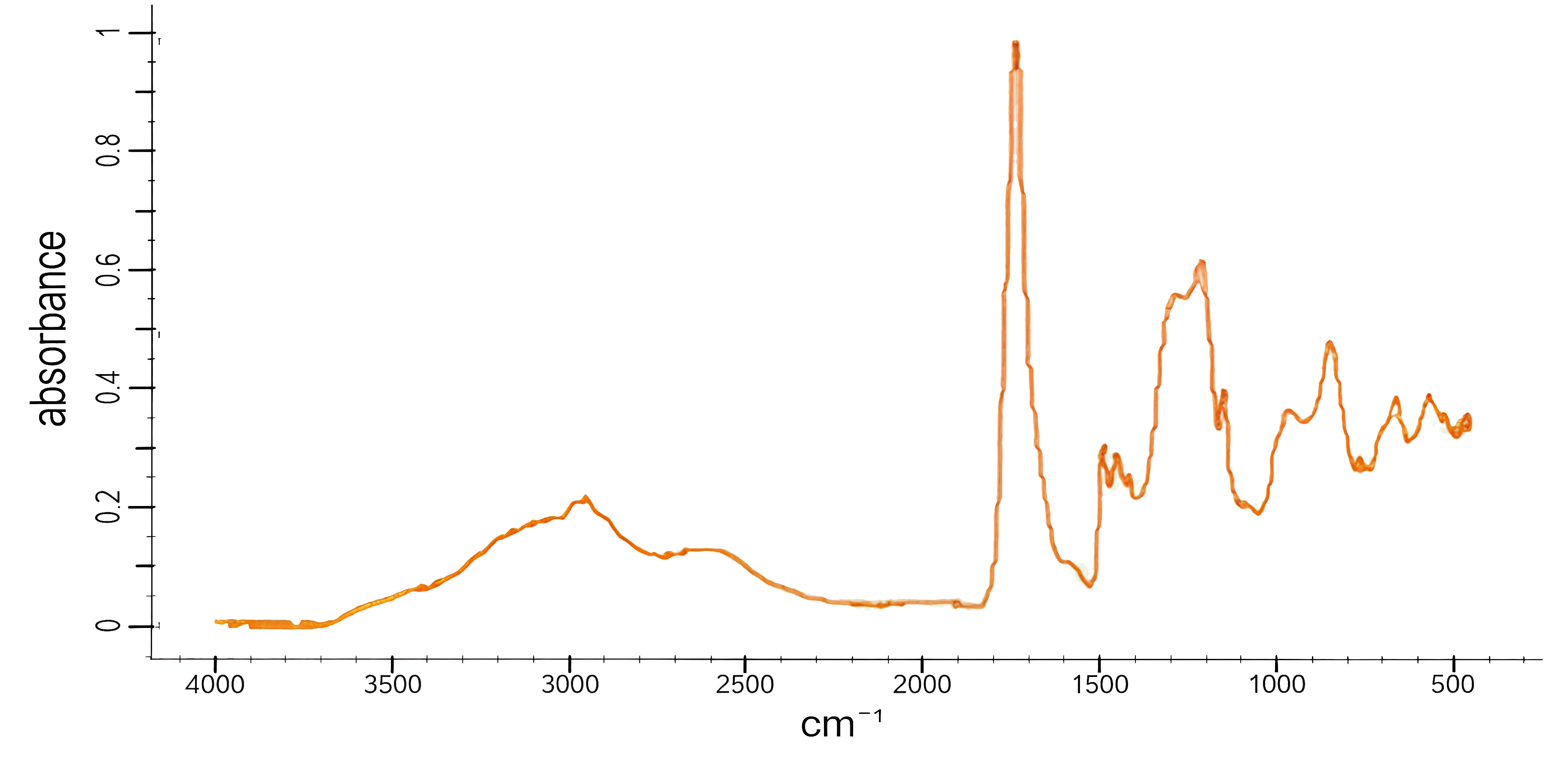
- Спектр 3
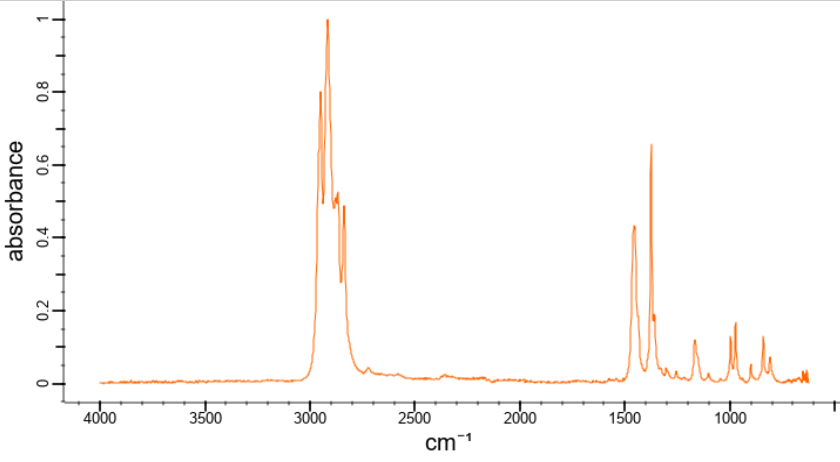
- Спектр 4
Полимеры:
- Полистирол (ПС).
- Полиакриловая кислота (ПАК).
- Полиэтилентерефталат (ПЭТФ).
- Полипропилен (ПП).
РешениеХарактерными полосами поглощения в данном случае являются интенсивная широкая полоса 2800–3600 см\(^{-1}\) (О–Н группа), 2900 см\(^{-1}\) (С–Н группа), 1650–1750 см\(^{-1}\) (С=О группа), 700 см\(^{-1}\) (фенильная группа). Таким образом, для первого полимера ожидается полоса фенильной группы, для второго ОН и СО полосы, для третьего — СО, для четвертого — СН.
ОтветCBAD.
Назовите химические способы переработки нефти.
- Пиролиз.
- Фракционирование.
- Перегонка.
- Каталитический крекинг.
ОтветA, D.
Наилучшую детонационную устойчивость имеет бензин с октановым числом:
- 50,
- 96,
- 75,
- 82.
ОтветB (чем больше, тем устойчивее топливо).
Для каких из процессов характерны самые высокие температуры?
- Фракционирование.
- Каталитический крекинг.
- Термический крекинг.
- Пиролиз.
ОтветC, D.
В термическом крекинге из молекулы алкана может получиться (при условии образования лишь двух продуктов):
- алкан и алкен,
- алкан и алкан,
- алкан и бензол,
- два циклоалкана.
ОтветA.
- Условие
Используя поиск в интернете, ознакомьтесь со статьей и выберите НЕВЕРНЫЕ утверждения:
Рыжикова И. Г., Волков А. М., Бауман Н. А., Казаков Ю. М., Вольфсон С. И. Исследование физико-механических свойств смесей ПП/СКЭПТ, модифицированных пероксидом и системой пероксид/ТМПТА // Вестник Казанского технологического университета. 2013. №10.
- Все примененные составы модифицирующих систем показали увеличение показателя текучести расплава композиции по сравнению с немодифицированной системой ПП/СКЭПТ.
- Молекулярная масса используемого СКЭПТ оказывает влияние на ударную вязкость композиции ПП/СКЭПТ.
- Большее относительное удлинение при разрыве показывают композиции с низкомолекулярным СКЭПТ.
- Одним из факторов, оказывающим влияние на свойства композиций, модифицированных триметилолпропантриакрилатом, является ускорение сшивания звеньев полипропилена и этилен-пропиленового каучука.
ОтветD.
- Условие
Используя поиск в интернете, ознакомьтесь со статьей и выберите ВЕРНОЕ утверждение:
DOI статьи 10.1016/j.polymer.2020.122341
- Использовалась сверточная нейронная сеть, оперирующая непосредственно кодами SMILES в качестве входных данных.
- Относительные ошибки и для обучающего, и для тестового наборов данных составили около 6%.
- В функции потерь авторы применяют среднеквадратичную ошибку между предсказанными и реальными температурами стеклования.
- Для генерации предсказания с помощью полученной модели необходимо использовать следующие входные данные для каждого прогнозируемого образца: химическая структурная формула, молекулярно-массовое распределение, температура стеклования.
ОтветB.
В реакторе при контролируемом давлении газообразного мономера проводили реакцию полимеризации. В ходе исследования кинетики процесса были получены следующие данные, см. таблицу 2.
| Время, ч | 1,5 | 2 | 2,5 | 3 | 3,5 | 4 | 4,5 | 5 |
|---|---|---|---|---|---|---|---|---|
| \(P_t\), кПа | 126 | 110,7 | 102,2 | 87,6 | 67,8 | 44,4 | 27,2 | 17,9 |
Известно, что рост полимерной цепи связан с давлением мономера и описывается уравнением нулевого порядка: \[P_t = P_0 - k \cdot t.\]
Используя регрессионный анализ, рассчитайте константу скорости реакции роста цепи полимера в килопаскалях в час с точностью до одного знака после запятой.
Сделаем необходимые расчеты в Excel: используя диаграмму, построим линию тренда по полученным точкам и найдем значения коэффициентов полученной функции. Красным на рис. 1.16 выделено значение константы в килопаскалях в час.
\(32{,}6 \pm 0{,}1\) кПа/ч.